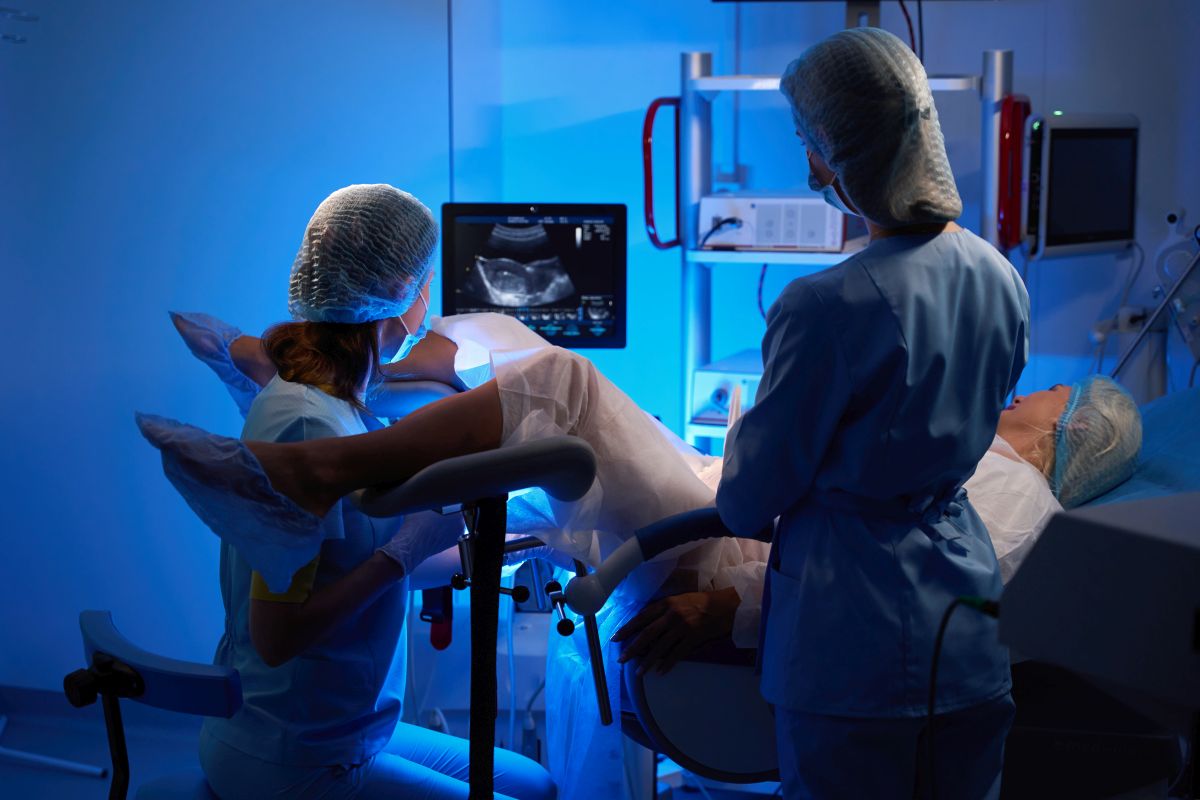
La vitrification embryonnaire consiste en une congélation ultra-rapide. Elle peut être réalisée lorsqu’aucun transfert embryonnaire n’a pas lieu après le développement des embryons, notamment si l’endomètre n’est pas dans les conditions idéales, mais également lorsque des embryons de bonne qualité restent disponibles après le transfert.
Ainsi, il est possible de préserver des embryons pour de futures tentatives, soit afin d’agrandir la famille, soit pour augmenter les chances de succès en cas d’échec du premier transfert.
La biopsie embryonnaire est réalisée dans les cas où le traitement inclut un Diagnostic Génétique Préimplantatoire (DPI/PGT).
Cette technique consiste, au stade de blastocyste, à prélever 3 à 5 cellules du trophectoderme, c’est-à-dire de la partie qui formera le placenta. Ainsi, la partie destinée à devenir le bébé n’est pas impactée.
Une fois les cellules prélevées, l’embryon est vitrifié et conservé au centre de fertilité, tandis que les cellules prélevées sont analysées par le laboratoire de génétique. Lorsque les résultats sont disponibles, le transfert est décidé en fonction des embryons sains identifiés.
De nos jours, le diagnostic génétique préimplantatoire est l’une des techniques les plus courantes pour analyser le patrimoine génétique des embryons et évaluer leur viabilité. En effet, la majorité des anomalies génétiques entraînent soit un test de grossesse négatif, soit une fausse couche précoce. Étant donné la forte charge émotionnelle que représente un traitement de procréation assistée, ce type de test est de plus en plus demandé afin de réduire les épreuves émotionnelles associées.