Le diagnostic génétique préimplantatoire (DPI), également connu sous le sigle PGT (pour Preimplantation Genetic Testing), est une technique avancée, complémentaire à un traitement de fécondation in vitro (FIV) ou de don d’ovocytes, qui a pour objectif de détecter les altérations génétiques ou chromosomiques des embryons afin d’éviter le transfert d’embryons porteurs de ces anomalies.
De cette manière, seuls les embryons sains, sans anomalies génétiques, sont transférés, ce qui augmente les chances d’obtenir une grossesse viable et la naissance d’un bébé en bonne santé.
Le Diagnostic Génétique Préimplantatoire (DPI/PGT)

Le Diagnostic Génétique Préimplantatoire (DPI/PGT)
Diagnostic Génétique Préimplantatoire (DPI/PGT)
Les types de DPI/PGT
1. Le Diagnostic Génétique Préimplantatoire des aneuploïdies (PGT-A)
Également appelé PGT-A (Preimplantation Genetic Testing for Aneuploidy), auparavant connu sous le nom de PGS (Preimplantation Genetic Screening).
Le caryotype humain comporte 23 paires de chromosomes, soit 46 chromosomes au total et l’objectif de cette technique est d’identifier les embryons présentant des anomalies chromosomiques numériques, telles que des trisomies (3 chromosomes au lieu de 2) ou des monosomies (1 chromosome au lieu de 2), afin d’en éviter le transfert. Ainsi, en transférant uniquement des embryons chromosomiquement normaux, on réduit le risque de fausse couche et d’échec d’implantation, puisque la majorité des embryons porteurs d’anomalies ne mèneront pas à la naissance d’un bébé en bonne santé.
2. Le Diagnostic Génétique Préimplantatoire des maladies monogéniques (PGT-M)
Le PGT-M a pour but d’identifier les embryons porteurs d’une mutation génétique pathogène responsable d’une maladie monogénique ou moléculaire, telles que la mucoviscidose (fibrose kystique), la dystrophie musculaire de Duchenne ou encore la maladie de Huntington.
La réalisation d’un PGT-M implique un délai supplémentaire dans le processus de traitement, car il est nécessaire d’effectuer au préalable des tests génétiques spécifiques, tels que le test d’informativité, réalisé à partir d’un échantillon de sang. Ce test permet de déterminer si les variants génétiques peuvent être identifiés dans les embryons analysés et ainsi distinguer avec précision les embryons atteints, porteurs ou sains. Dans certains cas, notamment pour certaines maladies, l’autorisation de la Commission Nationale de Reproduction Humaine Assistée (CNRHA) est requise pour évaluer la situation.
C’est cette commission qui approuve ou non la sélection embryonnaire, en fonction de l’histoire clinique, des antécédents génétiques et de la gravité de la maladie. Cette étape peut prolonger le temps nécessaire au traitement, car elle exige la collecte d’informations médicales détaillées et des délais d’attente pour la réponse officielle de la CNRHA.
L’avancée de cette technique a été déterminante pour les couples présentant un risque de transmission de maladies génétiques héréditaires à leurs enfants.
Quan est-il indiqué?
1. Le Diagnostic Génétique Préimplantatoire des aneuploïdies (PGT-A)
Les altérations génétiques chromosomiques, c’est-à-dire les aneuploïdies (modifications du nombre de chromosomes), sont étroitement liées aux anomalies génétiques d’origine ovocytaire, en raison de plusieurs facteurs biologiques associés au vieillissement des ovocytes. À mesure que les ovocytes vieillissent, des dommages s’accumulent dans l’ADN, et durant le processus de méiose, essentiel pour la séparation correcte des chromosomes, l’efficacité diminue. Cela peut entraîner des erreurs dans la répartition chromosomique, conduisant ainsi à des aneuploïdies chez les embryons.
C’est pourquoi le PGT-A est particulièrement indiqué dans les cas suivants :
-
Âge maternel avancé : un âge maternel supérieur à 35 ans s’accompagne d’une augmentation du risque d’anomalies génétiques, qui devient plus marquée à partir de 37 ans. Cela est dû au fait que, lors de la formation des ovocytes, le mécanisme de division cellulaire perd en précision avec le temps, augmentant ainsi le risque de produire des ovocytes présentant des anomalies chromosomiques.
- Avortements spontanés à répétition : les patientes ayant des antécédents d’avortements spontanés récurrents peuvent bénéficier d’un PGT-A afin de sélectionner des embryons présentant une dotation chromosomique normale, car ces fausses couches peuvent avoir une origine génétique.
- Échecs répétés de fécondation in vitro (FIV) : chez les patientes ayant déjà suivi plusieurs cycles de FIV sans succès, sans qu’un diagnostic génétique ait été réalisé, les aneuploïdies embryonnaires peuvent être à l’origine des échecs d’implantation.
-
Amélioration de l’efficacité du traitement : le PGT-A peut également être indiqué pour les patientes souhaitant optimiser les résultats du traitement, réduire les délais, augmenter les taux d’implantation et diminuer le risque de fausse couche.
2. Le Diagnostic Génétique Préimplantatoire des maladies monogéniques (PGT-M)
Le PGT-M est indiqué chez les patientes porteuses de maladies génétiques spécifiques causées par une mutation dans un gène :
- Antécédents familiaux de maladies génétiques : les patientes ayant des antécédents familiaux de maladies génétiques telles que la fibrose kystique ou la dystrophie musculaire de Duchenne.
- L’un des parents est porteur connu d’une maladie génétique..
Comment se réalise le DPI?
Tout d’abord, il est important de souligner que la réalisation d’un PGT nécessite la présence de personnel qualifié et expérimenté dans le laboratoire de fécondation in vitro.
1. Le développement embryonnaire
Après la fécondation, les embryons se développent en laboratoire jusqu’au 5ᵉ-6ᵉ jour, atteignant le stade de blastocyste, moment où la biopsie embryonnaire est réalisée. Actuellement, il est préférable d’effectuer la biopsie au stade de blastocyste, car il y a quelques années, elle se pratiquait au 3ᵉ jour de développement embryonnaire, lorsque l’embryon comptait 8 à 9 cellules. À ce stade, on retirait une seule cellule pour l’analyse, ce qui posait souvent un problème : en raison de la faible quantité de matériel génétique, il n’était parfois pas possible d’obtenir un résultat fiable (échec d’amplification).
Grâce aux progrès de la culture embryonnaire, il est désormais possible de maintenir les embryons jusqu’au stade de blastocyste, où ils comptent environ 200 cellules. Cela permet de prélever une quantité plus importante de matériel génétique sans compromettre la viabilité de l’embryon.
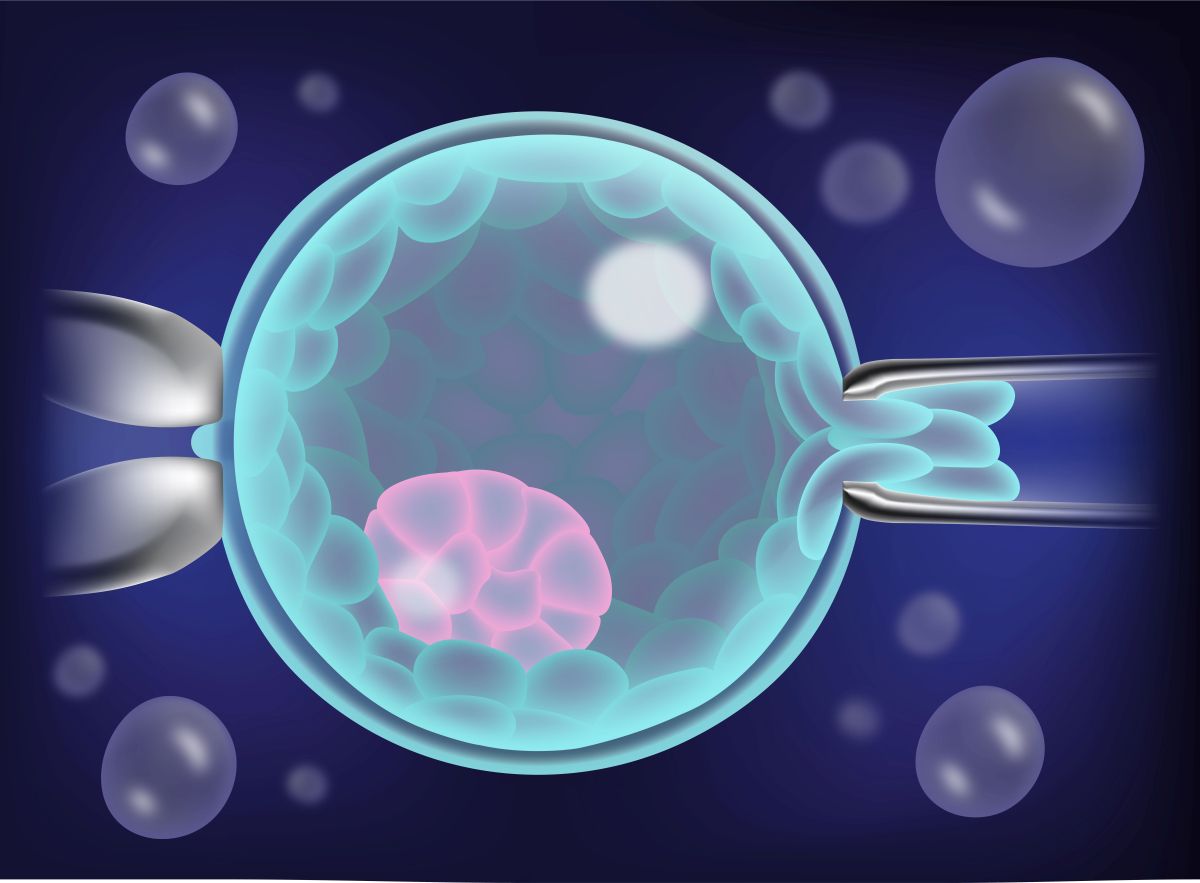
2. La biopsie embryonnaire
La biopsie embryonnaire est la procédure au cours de laquelle des cellules sont extraites de l’embryon afin d’être analysées et de détecter d’éventuelles anomalies génétiques.
Comme mentionné précédemment, le moment idéal pour effectuer la biopsie est le stade de blastocyste, car il permet d’extraire un plus grand nombre de cellules pour l’analyse, offrant ainsi une plus grande précision. De plus, l’analyse d’une quantité plus importante de matériel génétique permet d’identifier la présence éventuelle de mosaïcisme, c’est-à-dire la coexistence de deux lignées cellulaires différentes : l’une normale et l’autre présentant une altération génétique. Une biopsie réalisée au 3ᵉ jour ne permettrait pas de détecter cela, puisqu’elle ne disposerait que d’une seule cellule.
Par ailleurs, la biopsie au stade de blastocyste permet également de réduire le coût économique du traitement, car seuls les embryons ayant atteint ce stade (ceux ayant un réel potentiel de donner lieu à une grossesse) sont biopsiés.
Il est important de souligner que, lors du processus de biopsie embryonnaire, 4 à 5 cellules sont prélevées du trophectoderme, c’est-à-dire de la structure qui formera le placenta. La masse cellulaire interne, qui donnera naissance au bébé, n’est jamais impactée.
La perforation de la zone pellucide
Les ovocytes, dès le départ, sont entourés d’une couche protectrice appelée zone pellucide. Cette couche reste autour de l’embryon jusqu’à son implantation dans l’utérus après l’éclosion. Cependant, pour réaliser la biopsie, il est indispensable de pratiquer un petit orifice afin d’accéder aux cellules à l’intérieur.
Cette perforation est appelée Éclosion Assistée ou Assisted Hatching, et peut être réalisée au moment de la biopsie, ou, plus fréquemment, quelques jours avant, afin de permettre à l’embryon de commencer à sortir de sa couche protectrice et ainsi faciliter le processus de biopsie. Cet orifice est généralement réalisé à l’aide d’une technologie laser.
L’extraction des cellules
Une fois que le blastocyste est sorti de la zone pellucide, ou du moins en partie, l’embryon est maintenu sous microscope à l’aide d’une pipette, manipulée par l’embryologiste au moyen d’un micromanipulateur. Une fois l’embryon stabilisé, une autre fine pipette, dirigée par un second micromanipulateur, aspire 4 à 5 cellules à l’intérieur du capillaire. Lorsque celles-ci sont à l’intérieur, un pointeur laser est utilisé pour rompre les jonctions intercellulaires, séparant ainsi les cellules de l’embryon.
La mise en tube des cellules
Une fois les cellules extraites, on procède à la mise en tube (tubbing), c’est-à-dire qu’elles sont conditionnées dans un tube et envoyées à un laboratoire spécialisé pour analyse génétique.
La vitrification des embryons
Après la biopsie des embryons et la conservation des cellules destinées à l’analyse génétique, les embryons sont vitrifiés et conservés dans un réservoir d’azote liquide, en attente des résultats de l’analyse afin de sélectionner l’embryon ou les embryons sains et sans anomalies.
L’analyse génétique des cellules biopsiées
L’analyse génétique peut être réalisée à l’aide de différentes techniques qui ont évolué au fil des années.
Actuellement, la méthode la plus utilisée est la réaction en chaîne par polymérase (PCR), combinée au séquençage de nouvelle génération (NGS), ce qui permet de détecter un grand nombre d’anomalies génétiques.
Les résultats de l’analyse génétique
Une fois que le centre de fertilité reçoit les résultats de l’analyse génétique des embryons, ceux qui ne présentent pas d’altérations génétiques sont sélectionnés pour être transférés dans l’utérus de la patiente.
Il peut arriver que tous les embryons biopsiés et analysés présentent une anomalie génétique. Dans ce cas, aucun embryon ne pourrait être transféré. Dans de telles situations, une consultation approfondie est réalisée afin d’évaluer les possibilités d’un nouveau traitement, d’analyser les informations fournies par les résultats, et de considérer d’autres options offrant de meilleures garanties de succès, comme le don d’ovocytes.
C’est pourquoi un diagnostic génétique est essentiel pour déterminer les prochaines étapes. En effet, dans une situation où les embryons auraient été transférés sans analyse génétique préalable, cela aurait pu aboutir à un test de grossesse négatif ou à une fausse couche, sans connaître la cause sous-jacente.
Cependant, il est important de noter que le transfert d’un embryon euploïde, c’est-à-dire génétiquement normal, ne garantit pas une grossesse. D’autres facteurs, tels que la réceptivité de l’endomètre, les facteurs immunologiques ou même anatomiques, peuvent également influencer de manière significative le résultat du traitement.
Un doute? N’hésitez pas à nous appeler au +34 848 640 650
Vous pouvez également nous joindre à travers le formulaire suivant. Nous prendrons contact avec vous le plus rapidement possible.
Otros Tratamientos de Reproducción Asistida
Además del Diagnóstico Genético Preimplantacional (DGP/PGT), existen otros tratamientos de reproducción asistida que pueden ayudar a cumplir el sueño de tener un hijo, como la fecundación in vitro (FIV), la ovodonación o la inseminación artificial, entre otros.
Cada tratamiento es personalizado según las necesidades de los pacientes. Si estás buscando orientación sobre el mejor camino a seguir, no dudes en ponerte en contacto con nosotros para recibir una atención personalizada y profesional.

Inseminación Artificial (IA)
La inseminación artificial (IA) es el tratamiento de reproducción asistida más sencillo. Este consiste en introducir la muestra de espermatozoides directamente en el útero de la mujer.

Fecundación In Vitro (FIV)
La fecundación in vitro (FIV) consiste en la unión de los óvulos y espermatozoides dentro del laboratorio para generar embriones, que posteriormente serán transferidos al útero para su implantación y conseguir el embarazo.

Ovodonación
La ovodonación es un tratamiento en el que se lleva a cabo una fecundación in vitro (FIV), utilizando óvulos de una donante y que se combinan con una muestra de semen, ya sea de la pareja de la paciente o de un donante.
Esta empresa ha recibido una subvención del Gobierno de Navarra al amparo de la convocatoria de Fomento de la Empresa Digital Navarra 2025.



